Nous étudions la structure et les mécanismes moléculaires impliqués dans l'assemblage et dans la transmission virale.
1°) Virus de plante
La transmission des virus d'une plante à l'autre est principalement réalisée par un vecteur. Les vecteurs les plus connus sont les insectes, les nématodes ou les acariens. Deux modes d'interaction entre le virus et le vecteur doivent être différenciés. Le mode circulant qui est un mode ou le virus entre dans le vecteur par l'intestin, puis diffuse jusqu'aux glandes salivaires où il va être ensuite libéré dans la nouvelle plante lors de la nutrition du vecteur. Il est important de mentionner que certains virus arrivent a se répliquer dans le vecteur, d'autres pas. Il y a également le mode dit non-circulant où le virus reste attaché sur les parties buccales du virus avant d'être libéré dans une nouvelle plante au moment de la nutrition du vecteur.
Les mécanismes moléculaires impliqués dans ces modes de transmissions sont très peu connus, bien que les dégâts causés par les virus sur les cultures soient extrêmement importants. Ces dernières années, des études montrent de plus en plus que les produits utilisés dans la lutte phytosanitaire ont des impacts négatifs sur la faune mais également sur l'homme, pouvant ainsi par exemple favoriser certains cancers. Il est donc important d'étudier de nouvelles voies permettant de lutter contre la transmission des virus de plante.
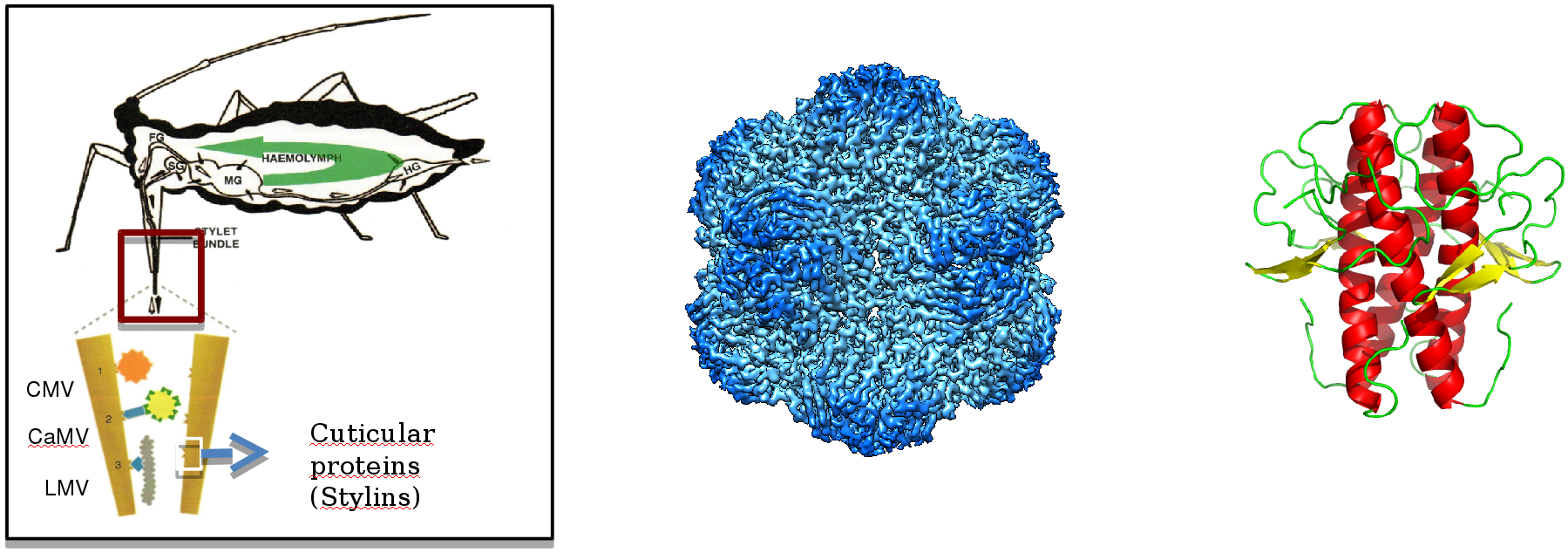
Jusqu'il y a peu, il était admis que la transmission non-circulante résultait d'une interaction aspécifique des virus avec les pièces buccales du vecteur. Or, il s'avère que cette interaction n'est pas du tout aspécifique mais résulte d'une interaction contrôlée entre les virus et des récepteurs protéiques. Dans ce contexte, nous étudions plus particulièrement la transmission des virus par les pucerons, qui sont responsables de la diffusion de très très nombreux virus de plante au travers le monde.
Collaborateurs:
Stéphane Blanc, Marilyne Uzest, Jean-Louis Zeddam CIRAD-INRA Montpellier
Véronique Brault, David Gilmer, Gérard Demangeat, INRA Colmar
Véronique Ziegler-Graaf, Christophe Ritzenthaler, IBMC, Strasbourg
Financements: Fondation Bill et Belinda Gates, ANR-Stylhook
2°) Virus humain
Nous étudions l’assemblage et les mécanismes de réplication de certains virus par des approches de tomographie et de cryo-tomographie électronique.
Etude fonctionnelle et structurale des organelles membranaires hébergeant la réplication du virus Chikungunya dans les cellules humaines
Le virusChikungunya est un arbovirus responsable chez l’homme d’un syndrome aigu pouvant évoluer vers des arthralgies chroniques invalidantes. Notre objectif vise à définir l’organisation structurale des compartiments membranaires hébergeant les complexes de réplication viraux et à identifier les interactions hôte-pathogène impliquées dans la biogenèse de ces compartiments par une approche intégrée basée sur des techniques de crible génétique, d’analyses fonctionnelles, de cryo-microscopie corrélative et de cryo-tomographie électronique.
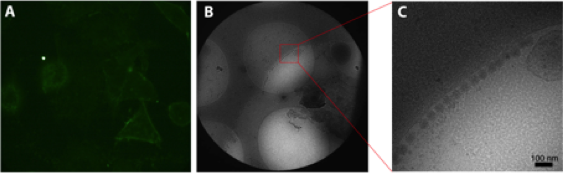
Collaborateurs: Laurence Briant, Jean-Luc Battini, IRIM Montpellier
Financement: ANR-Tomochikv
Séquence et structure des signaux d'empaquetage du génome de virus influenza A
Les virus influenza A (VIA) sont responsables d'épidémies grippales saisonnières et occasionnellement de graves pandémies. La segmentation des génomes grippaux en 8 ARN viraux (ARNv) (-) facilite l'évolution rapide des virus et l'émergence des virus pandémiques par réassortiment génétique mais complique leur assemblage. En effet, pour être infectieux, les virions doivent empaqueter au moins une copie de chaque ARNv. Le consensus actuel est que les ARNv sont empaquetés de manière sélective dans les particules virales. Bien que ce modèle ait des implications importantes pour le réassortiment génétique et la production de vaccins, les mécanismes moléculaires d'empaquetage spécifique restent méconnus. Des signaux d'empaquetage ont été identifies sur chacun des ARNv mais seulement de manière grossière et incomplète.
Le but de notre projet est de déchiffrer les mécanismes moléculaires qui gouvernent l'empaquetage du génome des virus Influenza A (VIA) et comprendre leur impact sur l'organisation spatiale des ARNv.

En plus de son intérêt fondamental, ce projet impactera, à long terme, la santé humaine - et animale - car il permettra d'améliorer le processus de production de vaccins et aidera à prédire l'émergence de souches virales pandémiques
Collaborateurs:
Roland Marquet, IBMC, Strasbourg
Manuel-Rosa Calatrava, VirPAth, Lyon
Prof. Dr. Martin Schwemmle, Institute of Virology, Freiburg, Germany.
Financement: ANR-PsiFlu

